Covid. Ferri: pensiamo a prevenire la prossima pandemia
 Dobbiamo entrare nell’ottica di istituire programmi di sorveglianza epidemiologica e genomica. Solo così potremo evitare che un nuovo Coronavirus ci colpisca come ha fatto Sars-Cov-2
Dobbiamo entrare nell’ottica di istituire programmi di sorveglianza epidemiologica e genomica. Solo così potremo evitare che un nuovo Coronavirus ci colpisca come ha fatto Sars-Cov-2
La pandemia di Covid-19 è la sesta crisi sanitaria globale dalla pandemia influenzale del 1918 e la sua comparsa, interamente ricondotta alle attività umane, ha evidenziato quanto la nostra società sia estremamente vulnerabile, quando si verificano eventi imprevisti di malattie infettive. Covid-19 ci ha anche indicato la strada per essere più attrezzati, in un mondo globalizzato e tecnologico, ad affrontare le future emergenze pandemiche ed ha segnalato l’importanza di guardare e monitorare l’interfaccia animali-ambiente-uomo, da cui possono derivare salti di specie o spillover, come molto probabilmente è avvenuto con il passaggio di Sars-Cov-2 (l’agente di Covid-19) dai pipistrelli all’uomo.
Partiamo dal dato che la maggior parte delle malattie emergenti provengono dagli animali e che generalmente, anche in presenza di sistemi allenati di sanità pubblica, vengono diagnosticate in ritardo rispetto alla notifica dei focolai di infezione umana. Ed è quello che è avvenuto nelle prime fasi di questa pandemia e delle precedenti, dove il ricorso alla sola diagnosi clinica seppure tempestiva, si è dimostrato insufficiente ad arginare e controllare il decorso epidemico. E’ vero invece che, in presenza di nuovi rischi a carattere globale, è fondamentale sviluppare programmi proattivi di sorveglianza epidemiologica e genomica basati sul riconoscimento precoce delle sindromi di malattie insolite e sulla individuazione di serbatoi animali (trasmissione pre-diagnostica) di patogeni che si trasmettono all’uomo, ancor prima della loro individuazione nei casi clinici umani. Queste attività devono trovare ideale collocazione all’interno di programmi di previsione ed intelligence pandemica, e in una prospettiva One Health – la salute unica di uomo, animali ed ambiente – facilitare l’integrazione delle diverse professionalità che operano nel campo sanitario e non solo, e capitalizzare il dato di un’accelerazione significativa della sorveglianza genomica durante questa pandemia, con una scala di sequenziamento senza precedenti e la condivisione globale del genoma di SARS-CoV-2, che hanno superato l’influenza, l’HIV ed i patogeni di origine alimentare.
Nonostante l’ampio range di specie animali, selvatiche e domestiche, recettive ai coronavirus, ad oggi solo sette coronavirus, compreso SARS-CoV-2, hanno superato la barriera di specie per diventare patogeni umani ben consolidati. Se SARS-CoV-2 ha una probabile origine da un serbatoio animale, cosi come il 60% dei patogeni che causano malattie umane e il 75% dei patogeni umani emergenti, appare prioritario da un lato perfezionare la conoscenza sulla diversità degli agenti patogeni, in particolare dei virus e delle frequenze con cui si trasmettono all’uomo, dall’altra analizzare le complesse interconnessioni tra specie, ecosistemi e società umana, compresi l’ecologia dei serbatoi animali e dei fattori o drivers antropogenici (cambiamenti climatici, deforestazione, diminuzione della biodiversità ecc..) alla base dei processi globali che innescano l’insorgenza e la diffusione delle epidemie infettive.
Le infezioni Ebola, Sars, virus Zika e influenza aviaria per citarne alcune, si sono trasmesse all’uomo a partire da serbatoi animali, favoriti da fattori umani ed ambientali. Sebbene sia difficile prevedere con precisione l’intervallo di tempo di un evento di diffusione di un agente patogeno, si possono indagare i drivers antropogenici che segnalano le aree geografiche o hot spot, in cui i virus emergenti mostrano la tendenza a superare la barriera di specie ed avvicinarsi all’uomo. L’Oms ha individuato un elenco di dieci infezioni prioritarie che, a causa del loro potenziale epidemico e/o assenza o insufficienza di contromisure, rappresentano un rischio maggiore per la sanità pubblica e si è impegnata a definire i percorsi di ricerca e sviluppo per ciascuna di esse. Tra queste c’è l’infezione X causata da un nuovo patogeno, ancora sconosciuto ma con un potenziale pandemico ed in grado di minacciare la sicurezza sanitaria globale. COVID-19 ha fornito la prova della prima occorrenza della malattia X da quando è stata stabilita la sua designazione, emergendo molto prima del previsto.
La circolazione dei coronavirus correlati a SARS-CoV-2 nei pipistrelli
Individuare l’origine di SARS-CoV-2 significa indagare la diversità dei coronavirus animali e più specificamente di quelli SARS-CoV-2 correlati nei pipistrelli, la cui distribuzione geografica è molto più ampia di quanto ritenuto in precedenza. In alcuni paesi del sud-est asiatico opera un programma di sorveglianza che, attraverso le analisi degli alberi genealogici dei coronavirus nei pipistrelli, punta ad intercettare ceppi potenzialmente pericolosi ed individuare i serbatoi animali su cui concentrare la ricerca. Un progetto simile per la ricerca genomica dei coronavirus nei pipistrelli, denominato DEEP VZN (Discovery & Exploration of Emerging Pathogens Viral Zoonoses), finanziato con 125 milioni di dollari da USAID si svolge opera nella stessa area geografica, ma anche in Africa, Asia e America Latina.
Di recente nel nord del Laos sono stati individuati tre coronavirus in pipistrelli della specie Rhinolophus spp., geneticamente più simili a SARS-CoV-2 rispetto al coronavirus RaTG13, e che presentano sulla proteina Spike un dominio di legame molto vicino a SARS-CoV-2 e, diversamente dagli altri coronavirus correlati, in grado di legarsi fortemente al recettore ACE2 delle cellule umane. Risultati simili sono confermati da un altro studio condotto in Thailandia nel 2021 in pipistrelli della specie Rhinolophus acuminatus. Questi dati segnalano la possibilità che SARS-CoV-2 abbia potuto acquisire la capacità di trasmissione interumana solo attraverso la selezione evolutiva naturale e smentiscono l’ipotesi del virus costruito in laboratorio. Pertanto, se la selezione è naturale l’origine deve essere cercata in serbatoi naturali.
La circolazione dei coronavirus in altre specie animali
Man a mano che gli studi di sorveglianza si arricchiscono di nuove evidenze, si estende la gamma di potenziali serbatoi animali di SARS-CoV-2. L’ultima specie, in ordine di tempo, trovata sensibile al virus è l’ippopotamo, molto probabilmente infettato dall’uomo, processo noto come antroponosi. E non può nemmeno essere esclusa la possibilità che gli animali possano ritrasmettere SARS-CoV-2 all’uomo (antroponosi inversa). I recenti episodi di infezione e deriva genetica/antigenica di SARS-CoV-2 nei visoni e la ritrasmissione del virus mutato (cluster 5) all’uomo, ne sono un chiaro esempio e, al contempo, un avvertimento.
Non si può escludere che eventi simili possano verificarsi con altre specie animali e che la formazione di un nuovo serbatoio non umano di SARS-CoV-2 possa estendersi ai mustelidi in cattività o altri animali selvatici, da cui il virus potrebbe ritornare all’uomo. Di particolare interesse è la suscettibilità all’infezione naturale SARS-CoV-2 del cervo a coda bianca. Da recenti indagini di siero-prevalenza svolte fra la popolazione di cervi, nella regione nord-orientale degli USA, nello Iowa, e più di recente in Canada, in ampie percentuali dei soggetti esaminati è stata trovata sia la presenza di anticorpi anti-SARS-CoV-2 che la positività al virus. Gli studi di sequenziamento genomico hanno rilevato la circolazione nei cervi di varianti umane di SARS-CoV-2, come la B.1.2 e B.1.311, risultato di frequenti eventi di spillover uomo-cervi e la trasmissione tra questi animali. Più preoccupante è il ruolo potenziale dei roditori come serbatoi di SARS-CoV-2 per la presenza sulla proteina Spike dei coronavirus a loro associati ai roditori del sito di scissione della furina, generalmente assente nei coronavirus dei pipistrelli, che può aumentare l’efficienza dell’infezione virale e la trasmissibilità.
Perché serve l’approccio One Health
Prove dirette dimostrano che la variante alfa o B.1.1.7 di SARS-CoV-2, e di altre varianti con la mutazione N501Y (es. la sudafricana e filippina) hanno acquisito la capacità di espandere il tropismo di specie ai murini. In una prospettiva One Health occorre dunque includere nella sorveglianza dei sarbecovirus (a cui appartiene SARS-CoV-2) anche i roditori, con cui l’uomo ha una convivenza strettissima ed è plausibile il rischio di infezione. In siffatto contesto di costante evoluzione epidemiologica dei coronavirus, analogamente a quanto accaduto per i visoni, preoccupa lo scenario di un rischio potenziale di reinfezione umana o di un ulteriore salto in una specie animale selvatica, come i pipistrelli, che possono fungere da nuovo serbatoio. Per le vaste implicazioni per il corso a lungo termine della pandemia COVID-19 e di quelle future, è inderogabile l’approccio One Health.
Cercare più virus ed ottenere la sequenza genomica sono passi fondamentali per definire la distribuzione geografica del rischio ed attuare programmi sorveglianza mirati. Ciò è rilevante per SARS-CoV-2 a causa della sua complessa evoluzione e dell’emergenza di nuove varianti. La diffusa circolazione di SARS-CoV-2 e di altri coronavirus, risultato dei cicli replicativi all’interno delle cellule umane ed animali, crea anche le condizioni per una possibile ricombinazione genetica di due virus all’interno della stessa cellula e la produzione di un nuovo virus ibrido, il quale nella peggiore delle ipotesi può essere più minaccioso dei precedenti. Ciò è già accaduto in Malesia dove otto bambini son stati infettati da un ceppo di coronavirus ibrido.
Il futuro della sorveglianza genomica
Le future pandemie si possono prevedere, prevenire e combattere integrando la sorveglianza genomica umana, tradizionalmente focalizzata sui casi clinici o sulle infezioni già conosciute, con quella degli animali (fauna selvatica e vettori) e dell’ambiente. Ciò richiede la creazione di una infrastruttura e competenze in grado di raccogliere ed analizzare campioni genomici umani (es. comunità, ospedali o laboratori), animali ed ambientali, compresi i macelli, acque reflue urbane, rifiuti animali ed i luoghi associati a un rischio più elevato di circolazione di agenti patogeni quali gli aerei a lunga distanza o stazioni della metropolitana. La necessità di sviluppare sistemi di sorveglianza genomica integrata era nelle intenzioni dell’OMS, FAO e l’OIE già nel 2004, quando le tre agenzie conclusero congiuntamente che le minacce emergenti di malattie infettive devono essere affrontate in una prospettiva One Health, implementando nuovi meccanismi e strumenti di sorveglianza come i sistemi di informazione geografica, dati di telerilevamento ed epidemiologia molecolare. Purtroppo, ciò non è servito a prevedere l’insorgenza della pandemia COVID-19. Se nella nuova definizione di One Health viene enfatizzato, a ragione, il ruolo dell’ambiente e dei relativi ecosistemi strettamente collegati e interdipendente con la salute delle persone e degli animali, la speranza è che la sua piena declinazione operativa, unitamente alle raccomandazioni formulate dai leader dell’UE, del G7 e del G20 in occasione dell’Assemblea Mondiale della Sanità nel maggio 2021, e la promessa di importanti investimenti da parte della Commissione Europea, per iniziative volte a rafforzare l’infrastruttura dedicata alle varianti della SARS -CoV2, possano fornire il terreno ideale per affrontare in modo proattivo le future minacce pandemiche.
Maurizio Ferri
Coordinatore scientifico SIMeVeP
Pubblicato su La Repubblica Salute il 30 dicembre
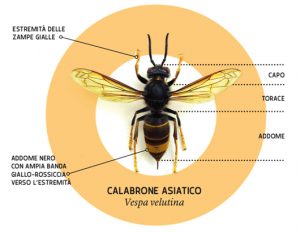 Aumentano le segnalazioni da parte degli apicoltori della provincia di Massa-Carrara per la presenza di Vespa velutina presso i loro apiari.
Aumentano le segnalazioni da parte degli apicoltori della provincia di Massa-Carrara per la presenza di Vespa velutina presso i loro apiari. Mentre i casi documentati d’infezione da SARS-CoV-2 ammontano a circa 300 milioni su scala planetaria, con oltre 5 milioni e mezzo degli stessi ad esito infausto (poco meno di 140.000 dei quali in Italia), la contagiosissima variante “Omicron” (alias “B.1.1.529”) impazza nei due Emisferi e nei cinque Continenti, preceduta dalla “Delta” ed affiancata dalle neogenite varianti “Deltaomicron” ed “Omicron 2” appena identificate, rispettivamente, a Cipro e in Danimarca.
Mentre i casi documentati d’infezione da SARS-CoV-2 ammontano a circa 300 milioni su scala planetaria, con oltre 5 milioni e mezzo degli stessi ad esito infausto (poco meno di 140.000 dei quali in Italia), la contagiosissima variante “Omicron” (alias “B.1.1.529”) impazza nei due Emisferi e nei cinque Continenti, preceduta dalla “Delta” ed affiancata dalle neogenite varianti “Deltaomicron” ed “Omicron 2” appena identificate, rispettivamente, a Cipro e in Danimarca. A un anno dall’inoculazione del primo vaccino anti Covid-19, sono ancora numerose le domande senza risposta contro la malattia. Soprattutto a causa delle varianti del virus. Per provare a dare qualche risposta i ricercatori dell’Istituto Zooprofilattico Sperimentale delle Venezie hanno condotto uno studio sulla mutazione Omicron, presentato durante una conferenza stampa del Governatore del Veneto Luca Zaia. Ricerca che mostrerebbe come il test sierologico per la conta degli anticorpi non avrebbe più lo stesso valore di prima.
A un anno dall’inoculazione del primo vaccino anti Covid-19, sono ancora numerose le domande senza risposta contro la malattia. Soprattutto a causa delle varianti del virus. Per provare a dare qualche risposta i ricercatori dell’Istituto Zooprofilattico Sperimentale delle Venezie hanno condotto uno studio sulla mutazione Omicron, presentato durante una conferenza stampa del Governatore del Veneto Luca Zaia. Ricerca che mostrerebbe come il test sierologico per la conta degli anticorpi non avrebbe più lo stesso valore di prima. Siamo orgogliosi di avere avuto l’onore di ospitare a Roma questa importante iniziativa che si conclude con un documento di 33 punti in cui si rinnova l’impegno già emerso nel recente Global Health Summit affinché si possa “aumentare e diversificare la capacità produttiva di vaccini globale, locale e regionale, sviluppando competenze per i Paesi a reddito medio-basso.
Siamo orgogliosi di avere avuto l’onore di ospitare a Roma questa importante iniziativa che si conclude con un documento di 33 punti in cui si rinnova l’impegno già emerso nel recente Global Health Summit affinché si possa “aumentare e diversificare la capacità produttiva di vaccini globale, locale e regionale, sviluppando competenze per i Paesi a reddito medio-basso.
 Baylisascaris procyonis è un nematode endemico del Nordamerica e sporadicamente segnalato in altri Paesi: in Italia è stato segnalato per la prima volta nel 2021 da 5 procioni abbattuti nel territorio del Casentino (AR).
Baylisascaris procyonis è un nematode endemico del Nordamerica e sporadicamente segnalato in altri Paesi: in Italia è stato segnalato per la prima volta nel 2021 da 5 procioni abbattuti nel territorio del Casentino (AR). OIE – World Organisation For Animal Health -, Ministero della Salute e la rete degli Istituti Zooprofilattici Sperimentali (IIZZSS) hanno siglato un accordo per unire le forze e affrontare le sfide su One Health.
OIE – World Organisation For Animal Health -, Ministero della Salute e la rete degli Istituti Zooprofilattici Sperimentali (IIZZSS) hanno siglato un accordo per unire le forze e affrontare le sfide su One Health. Il Laboratorio di batteriologia speciale della sezione di Treviso dell’Istituto Zooprofilattico Sperimentale delle Venezie (IZSVe) ha identificato e dato il nome a una nuova specie di stafilococco.
Il Laboratorio di batteriologia speciale della sezione di Treviso dell’Istituto Zooprofilattico Sperimentale delle Venezie (IZSVe) ha identificato e dato il nome a una nuova specie di stafilococco.